Genska terapija: Premik paradigme pri hemofiliji
Namen satelitskega simpozija o genski terapiji (v sklopu
kongresa Evropskega združenja za hemofilijo in sorodne motnje – EAHAD 2022), v
organizaciji družbe CSL Behring, pri hemofiliji, je bil raziskati dosedanje in
prihajajoče okolje zdravljenja hemofilije s poudarkom na genski terapiji.
Kateri so možni izzivi ter morebitne napačne predstave v zvezi z gensko
terapijo ter kaj je potrebno za njeno uspešno implementacijo v klinično prakso?
Cilj simpozija je zagotoviti boljše razumevanje potenciala in praktičnih
vidikov te paradigme transformativnega zdravljenja za osebe s hemofilijo.

Izboljšave pri zdravljenju hemofilije skozi zadnja
desetletja so nedvomno spremenile življenja oseb, ki živijo s to boleznijo.
Nadomestna terapija faktorjev s podaljšanim delovanjem marsikomu danes prinaša bistveno
bolj “normalen” življenjski slog, prav tako tudi njegovo izboljšano upravljanje
hemofilije, “podaljšan režim” profilakse pa ponuja večjo fleksibilnost kar se
tiče doziranja faktorja, višji so tudi spodnji nivoji manjkajočega faktorja ter
na ta način izboljšani klinični izidi. In kako danes izgleda prihodnost
zdravljenja hemofilije? V bližnji prihodnosti bodo osebe s hemofilijo imele še več
možnosti zdravljenja. Skupne odločitve o najboljšem poteku obvladovanja
hemofilije bodo sprejemale osebe s hemofilijo ter njihov multidisciplinarni
zdravstveni tim. Nedvomno ostaja aktualno nadomestno zdravljenje, več poudarka in novih produktov se
pričakuje npr. pri nenadomestnem (nefaktorskem) zdravljenju ter seveda pri
genski terapiji.

Kje smo pri zdravljenju hemofilije danes? Standard oskrbe za hemofilijo je vseživljenjsko zdravljenje z nadomeščanjem koagulacijskega faktorja. Osebe s hemofilijo običajno potrebujejo “kronično” terapijo za preprečevanje večjih krvavitev, pojasnjuje Anette von Drygalski z Univerze Kalifornija, San Diego, ZDA, profesorica klinične medicine na Oddelku za hematologijo/onkologijo ter direktorica Centra za zdravljenje hemofilije in tromboze.
Profilaktično (redno) nadomeščanje faktorja je standard oskrbe pri težki obliki hemofilije za preprečevanje ali zmanjšanje števila krvavitev. Epizodno (po potrebi) nadomeščanje faktorja se danes še vedno prakticira pri hemofilikih za zdravljenje epizod krvavitev, npr. v času operativnega posega pri posamezniku.
Klinične smernice priporočajo profilakso pri težki obliki hemofilije A in B. Nekoliko se razlikujejo glede na posamezno geografsko področje, npr. za Evropo zapovedujejo “dostop” do profilakse pri tarčnem spodnjem nivoju faktorja med 3 in 5% ter posamezniku prilagojen režim zdravljenja. Cilj profilakse je osebam s hemofilijo omogočiti čimbolj zdravo, “normalno” življenje.
Profilaksa je namenjena ohranjanju hemostaze in
preprečevanju krvavitev, zlasti krvavitev v sklepe. O primarni profilaksi govorimo,
ko jo pričenjamo izvajati pri hemofiliku v zgodnjem otroštvu. Njen namen je, da
otrok doseže odraslo dobo brez okvar sklepov. Sekundarna profilaksa je
preventivno dodajanje faktorja po dveh ali več krvavitvah v določen sklep,
vendar pred pojavom dokazanega obolenja sklepov. Tu je namen omejiti posledice
nastalih sklepnih okvar. O terciarni profilaksi govorimo po pojavu radiološko
očitne bolezni sklepov. Pri tej pa je cilj upočasniti napredovanje sklepnega obolenja
pri hemofiliku ter reducirati bolečino in vzdrževati kvaliteto življenja
hemofilika - posameznika. Vendar pa tudi pri profilaktičnem zdravljenju obstaja
več različnih omejitev:
- tveganje za nastanek krvavitev še vedno obstaja;
- razvoj potencialnih inhibitorjev proti strjevalnemu faktorju;
- potreba po individualizaciji;
- potreba po venskem dostopu;
- družbeno breme (stigma);
To pomeni, da ob trenutnem standardu oskrbe obstajajo
številne nezadovoljene potrebe. Profilaksa lahko povzroči nihanje ravni
aktivnosti strjevalnega faktorja. Nizke najnižje ravni so povezane s prebojnimi
krvavitvami v sklepe. Venski dostop je pri tem lahko ovira za profilakso.
Razvoj inhibitorjev pa je največji zaplet pri nadomeščanju faktorja in je
povezan z dodatno obolevnostjo. Obvladovanje hemofilije pomeni
veliko ekonomsko breme za zdravstvene sisteme, stroški obvladovanja pa se povečujejo
s težavnostjo oblike bolezni, torej hemofilije. Osebe s hemofilijo nosijo
veliko breme zdravljenja, ki vpliva na njihovo vsakdanje življenje. Tako visoka
obremenitev (samo)zdravljenja lahko povzroči neoptimalno upoštevanje strokovnih
(hematoloških) navodil zaradi vrste dejavnikov:
- nenehno razmišljanje o zdravljenju;
- zamudnost pri apliciranju faktorja;
- pomanjkanje svobode;
- fizična obraba ven;
Nizka adherenca je povezana z naraščajočim številom
krvavitev in kronično bolečino. Nekatere osebe s hemofilijo so morda razočarane
nad njihovim trenutnim režimom zdravljenja:
- “potrebujem veliko časa, saj moram vsak teden razmišljati o svojem zdravljenju”;
- “zdravljenje preprečuje krvavitve, vendar se bolečina ne zdravi z injekcijami faktorja, naša bolečina vztraja”;
- “počutim se vkopanega, ne morem opraviti določenih stvari”;
- “način apliciranja zdravila je zelo invaziven in moteč”;
- “moje vene se rade prebijajo (“pokajo”);
- “zaradi tega moje življenje stoji na mestu”;
- “potreben je čas, veliko časa”;
- “staram se in težje najdem žilo za vbod”;
- “počutim se, kot da mi zdravljenje jemlje ogromno časa, in najti ves ta čas, da se dejansko usedem in to dejansko opravim, glede na moj urnik, je preprosto preveč”.
Napredek pri zdravljenju skozi zadnja desetletja, je
nedvomno izboljšal umrljivost in zmanjšal večje zaplete pri krvavitvah, vendar
enakost oz. pravičnost glede zdravja, primerljivega s splošno populacijo, ni
bila dosežena.
Greta Mulders, Erasmus Medical Centre, Rotterdam,
Nizozemska, medicinska sestra in koordinatorka, je predstavila psihosocialne
težave, ki so ključni del rezultatov, pomembnih za bolnika s hemofilijo.
Sporočila je, da “pravičnost” pri zdravju posameznika pomeni:
- preprečiti prezgodnjo smrt;
- izboljšati kakovost življenja in s tem sodelovanje pri vsakodnevnih dejavnostih;
- sposobnost opravljanja dejavnosti z nizkim tveganjem;
- neomejeno sodelovanje pri delu, karieri in družinskem življenju;
- bolj neomejen življenjski slog;
- neodvisnost od specializirane zdravstvene oskrbe;
- optimizirano zdravje in dobro počutje;
Ljudje s hemofilijo imajo težave z gibljivostjo sklepov, z
nepričakovanimi krvavitvami, bolečino ter negotovostjo pri vsakodnevnih
dejavnostih, kar vpliva tudi na njihovo izbiro hobijev. Hemofilija lahko
negativno vpliva na formalno izobraževanje, zaposlitev in izbiro poklica. Zato
je vloga medicinske sestre pri kakovosti življenja bolnika zelo pomembna, prav zaradi
obvladovanja psihosocialnega vpliva hemofilije pri trenutnem zdravljenju:
- dostopnost medicinskih sester;
- možnost posvetovanja;
- vodenje in podpora bolnikom: "Kako naj živim s hemofilijo?";
Kljub ustreznemu zdravljenju lahko osebe s hemofilijo
doživijo ter nosijo veliko psihosocialno breme. Pojavljajo se pogosta vprašanja:
- “kakšna je moja nevarnost za krvavitve danes?”;
- “imam danes čas za infuzijo?”;
- “ali sem uredil recept za faktor?”;
- “je moj počitniški kraj v bližini centra za zdravljenje hemofilije?”;
- “ali je to krvavitev ali artropatska bolečina v sklepu?”;
- “kako hemofilija vpliva na mojo družino?”;
- “ali lahko danes opravljam določeno dejavnost?”;
- “bom moral morda zamuditi šolo/službo?”;
Za boljšo oskrbo pri osebah s hemofilijo mora biti
zdravljenje celostno in multidisciplinarno, vključevati mora njihovo fizično,
socialno in psihično počutje. Izboljšanje enakosti/pravičnosti pri zdravju posameznika
vključuje pomoč bolniku, da se preusmeri na način razmišljanja, ki je bolj
pogosto odmaknjen od hemofilije. Miselnost odmaknjenosti od hemofiličnih
problemov bi lahko bila nedvomno nov cilj oskrbe v bodoče.
Michiel Coppens, internist vaskularne medicine in hemofilije,
Amsterdam University Medical Centre, Amsterdam, Nizozemska, je spregovoril o
izboljšanju oskrbe in optimizaciji rezultatov pri hemofiliji: Kaj nam prinaša
prihodnost?
Ko govorimo genski terapiji, ponavadi pričnemo z definicijo
oz. obravnavo AAV-ja (adeno-associated virus). AAV se iz naravno prisotnega
virusa spremeni v mehanizem dostave za gensko terapijo. Virusni vektorji
(najpogostejši AAV) so inaktivirani in nimajo sposobnosti razmnoževanja.
Monogene bolezni so dedna stanja, ki nastanejo zaradi mutacij v enem samem
genu. Med nje spada tudi hemofilija. Pri genski terapiji ne gre za “popravilo”
gena, pač pa za to, da je prava kopija gena “ustavljena” v AAV vektor, kateri
se usmeri v celice, ki pričnejo s produciranjem proteina (pri hemofilikih
manjkajočega faktorja za strjevanje krvi).
Hemofilija je nedvomno dobra kandidatka za gensko terapijo.
Hemofilija A in B, kot rečeno, spadata med monogene bolezni. Pri postopku
korekcije z gensko terapijo pri hemofiliji lahko pričakujemo veliko fenotipsko
izboljšanje po skromnem povečanju strjevalnega faktorja, pri čemer natančna
regulacija ni potrebna. Poleg tega je pomembna tudi učinkovitost, ki jo je možno zlahka
oceniti z meritvami ravni faktorjev in stopnjami krvavitev.
Napoveduje se, da bo genska terapija pri hemofiliji vplivala tudi na osnove genske terapije pri drugih boleznih, kar bo z njeno zasnovo ter pokazatelji glede njenih prednosti in slabosti v veliko pomoč drugim kliničnim raziskavam.
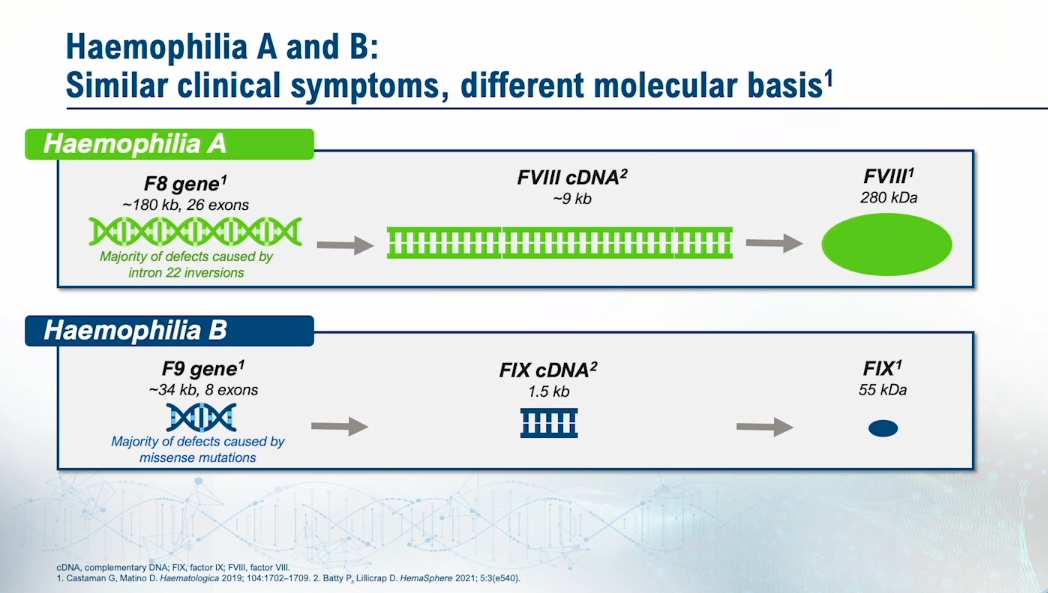
Pri genski terapiji je seveda razlika med genskim
zdravljenjem hemofilije A in hemofilije B, zaradi različne molekularne osnove.
Pri FVIII gre namreč za veliko večji protein kot pa pri FIX. To ima tudi
praktične posledice, kar je dobro vidno na naslednjem prikazu:
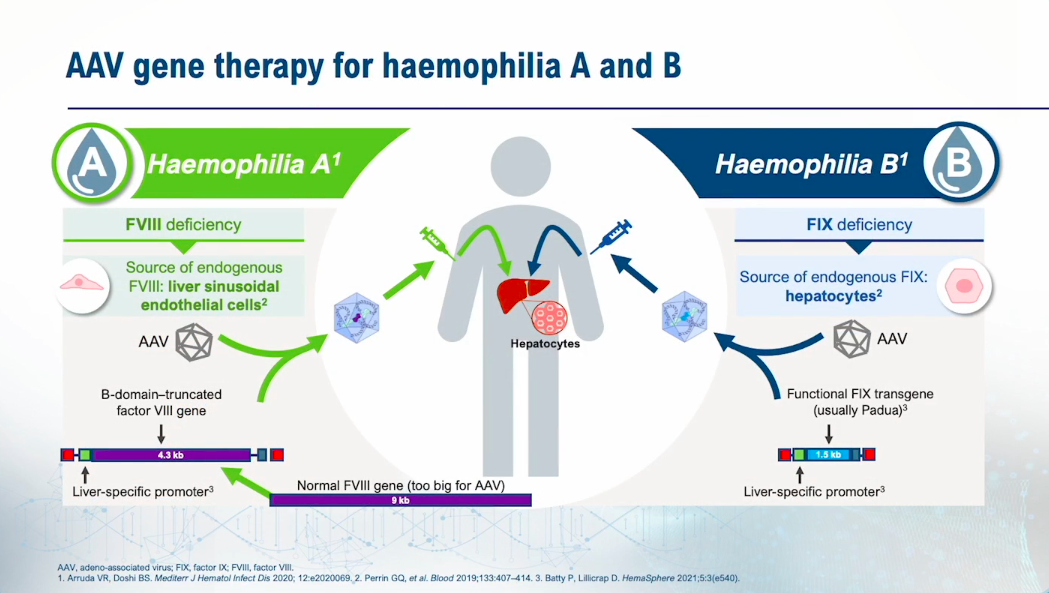
Na zgornji strani na levi vidite hemofilijo A, na spodnji levi strani pa dejansko lahko opazite, da je kopija DNK, potrebna za gensko terapijo, dejansko prevelika, da bi se prilegala v kapsido AAV-ja in šele po skrajšanju brisanja domene B lahko dobimo dovolj majhen zapis, da se dejansko prilega AAV kapsidi.
Na desni strani vidimo hemofilijo B, kjer je naravni vir proizvodnje FIX v istem tkivu večje velikosti, kot je bila tarča genske terapije, in ker je gen veliko manjši od gena FVIII, se zlahka prilega v AAV kapsido.
Kot je že znano, imamo v teku nekaj kliničnih študij, tako pri genski terapiji za hemofilijo A in B, nekatere od njih so se že premaknile v preizkusno fazo 3.
Če se osredotočimo zgolj na dve klinični študiji, ki sta že v fazi 3:
- GENE-r8: Valoctocogene roxaparvovec (hemofilija A), ki se izvaja pri osebah s težko obliko obolenja (pod 1% aktivnosti FVIII). Bolniki z že obstoječimi protitelesi proti naravni varianti AAV kapside so bili izključeni, ker je bilo pričakovano, da ti bolniki verjetno ne bodo pridobili primernega izraza genske terapije. Od 181 preverjenih oseb s hemofilijo A, je bilo 144 izbranih, od teh pa jih je 134 prejelo dozo genskega zdravljenja.
- HOPE-B: Etranacogene dezaparvovec (hemofilija B), se je klinično preizkušanje genskega zdravljenja izvajalo za osebe s pomanjkanjem FIX pod 2% aktivnosti. Zanimivo je, da je bilo v tem preskušanju dovoljeno vključiti in odmerjati bolnike z že obstoječimi protitelesi proti kapsidi AAV. Pregledanih je bilo skupno 75 bolnikov, od tega izbranih 67 ter nato prejemnikov končne doze genskega zdravljenja 54.
Če pogledamo rezultate za gensko terapijo pri hemofiliji A:
- kaže se trajna ekspresija endogenega FVIII pri posamezniku;
- profilaksa je bila ukinjena v 99% primerov (po opravljeni genski terapiji);
- zreducirala se je letna stopnja števila krvavitev za 84%;
- v 79-ih odstotkih pojava krvavitev, le-te niso bile dodatno zdravljene;
Če pogledamo še neželene dogodke:
- zvišanje transaminaz, ki zahteva zdravljenje s steroidi, je bilo potrebno pri 79 odstotkih udeležencev;
- pri 38 odstotkih prejemnikov genske terapije so se pojavili glavoboli, pri 37 odstotkih pa dodatna slabost;
Poglejmo razultate genskega zdravljenja pri hemofiliji B:
- večina udeležencev je bila na zdravljenje odzivna, vključno s tistimi, katerim so bila ugotovljena protitelesa na AAV5;
- rezultati so pokazali manjšo variabilnost z bolj stabilnim izražanjem faktorja;
- profilaksa je bila ukinjena pri 96 odstotkih udeležencev genskega zdravljenja;
- redukcija letne stopnje števila krvavitev je znašala 67%;
- pojav krvavitev ni zahteval dodatnega zdravljenja pri 81 odstotkih (v času prvih 6 mesecev po genskem zdravljenju) ter pri 83 odstotkih udeležencev (med šetim in dvanajstim mesecem po prejetju doze genske terapije);
- zvišanje transaminaz, ki zahteva zdravljenje s steroidi, je bilo potrebno pri 17 odstotkih udeležencev;
- pri 15 odstotkih prejemnikov genske terapije (hemofilija B) so se pojavili glavoboli, pri 13 odstotkih pa simptomi podobni gripi;
Vendar pa je v tem posebnem preskušanju en bolnik razvil
celični karcinom, ta dogodek je bil usmerjen na jetrno funkcijo. Seveda se
zadeva raziskuje, ali je dejansko dogodek povezan z opravljeno gensko terapijo
pri hemofiliji B ali ne.
Poglejmo si trajnost genske terapije, na podlagi kliničnih
razsikav v fazah 1 in 2. Pri genski terapiji hemofilije A je po približno 6
mesecih očiten vrhunec FVIII, potem pa se počasi niža in vprašanje je, ali bo
izražanje FVIII trajalo in kako dolgo se bo izgubila zaščita pred krvavitvijo
ter kdaj se bo izraz izgubil? Pri hemofiliji B se kaže stabilnost izražanja
FIX, celo po petih letih od prejetja doze genske terapije.
Kaj pa izkušnje bolnikov - udeležencev v testnih kliničnih fazah genske terapije za hemofilijo?
Predavateljev prvi pacient, ki je opravil gensko zdravljenje
v letu 2015 za hemofilijo B, je v preteklosti izgubil brata, prav tako hemofilika,
ki se je okužil s kontaminiranimi pripravki oz. plazemskimi produkti (okužba s HIV-om)
in nato umrl zaradi AIDS-a, leta 1989. 26 let kasneje je bil prvi nizozemski
hemofilik, pri katerem je bilo izvedeno gensko zdravljenje. Genska terapija torej
ima potencial, da spremeni življenje bolnikov, ne le z zmanjšanjem števila krvavitev,
ampak tako, da vodi posameznika v bistveno bolj "normalno” življenje.
V nadaljevanju je Greta Mulders predstavila pričakovanja
oseb s hemofilijo glede genske terapije ter opozorila, da morajo biti slednja
zelo previdno osnovana. Vedeti je potrebno:
- z gensko terapijo hemofilija ni ozdravljena;
- mutiran gen se še vedno lahko prenese na potomstvo;
- spremembe življenjskega sloga bodo po vsej verjetnosti potrebne;
- genska terapija ne bo odpravila poprejšnjih okvar sklepov pri hemofilikih;
- osebe se bodo morale prilagoditi monitoringu in testiranju po opravljeni genski terapiji;
- morda bo še vedno potrebna uporaba nadomestnih faktorjev (pri operativnih posegih ter večjih krvavitvah);
- vzdržnost genske terapije po obdobju 5-ih let trenutno še ni znana;
- po vsej verjetnosti ne bo mogoče ponovno opraviti genske terapije, ki bazira na AAV;
- pričakovani so stranski učinki zaradi ev. oslabitve
imunskega sistema pri posamezniku;
Kakšna vloga medicinske sestre se pričakuje v potencialu
genske terapije:
- več bo obiskov hemofilikov z novim zdravljenjem v primerjavi s standardno oskrbo;
- bolnike je treba informirati in razumeti njihovo zdravljenje;
- aktivno reagiranje in zdravljenje namesto čakanja kaj se bo zgodilo pri genski terapiji;
- stalna prisotnost medicinske sestre ter raziskovanje, kako se pacient počuti;
- vloga medicinske sestre se transformira od vloge učitelja do trenerja;
- zahteva po samozavesti in zaupanju v lastno telo in um;
- nova normalnost: bolniki se prilagajajo blagemu fenotipu hemofilije;
Osebam s hemofilijo po prejetju genske terapije je potrebno nuditi
ustrezno podporo:
- čustveno;
- psihološko;
- učno-izobraževalno;
Genska terapija za hemofilijo bo verjetno ustvarila “nov
razred” oseb s hemofilijo, ki je prešel iz težkega v blag fenotip bolezni in bo
potreboval drugačno zdravljenje kot npr. bolj tipičen posameznik z blago obliko
hemofilije.
Satelitski simpozij je vodil Giancarlo Castaman, Careggi
University Hospital, Firence, Italija, direktor Centra za motnje strjevanja
krvi in koagulacijo. Povedal je, da prihodnost genske terapije pri
hemofiliji danes prinaša:
- 52-tedenske podatke iz kliničnih preskušanj faze 3, o katerih so poročali za hemofilijo A in hemofilijo B;
- prve odobritve genske terapije s strani regulatorjev pričakujemo v prihodnjem letu;
- okoli genske terapije še vedno obstaja več neznank;
Hematološka strokovna združenja si nenehno prizadevajo za
izobraževanje in usmerjanje odločevalcev glede genske terapije pri hemofiliji,
kot so na primer:
- Evropsko združenje za hemofilijo in sorodne motnje (EAHAD);
- Ameriško hematološko društvo (ASH);
- Mednarodno društvo za trombozo in hemostazo (ISTH);
Delovna skupina za gensko terapijo pri EAHAD-u si prizadeva biti v ospredju pri zagotavljanju kritičnih informacij zdravnikom in bolnikom o genski terapiji.
Cilji delovne skupine EAHAD so:
- raziskati varnost genske terapije in parametre njenega izida;
- zagotavljanje posodobitev nedavnega razvoja genske terapije v smislu rezultatov in varnostni rezultatov;
- zbiranje podatkov o različnih preskušanjih, testih pri genski terapiji;
- obveščanje bolnikov in zdravstvenih delavcev;
Povzeto po: GENE THERAPY SATELLITE SYMPOSIUM - CSL BEHRING - GENE THERAPY: A PARADIGM SHIFT IN HAEMOPHILIA; EAHAD 2022
RB/HaemophAmicus









